在mRNA治疗领域,5′端帽结构(cap)长期被认为是翻译启动与分子稳定性的关键。然而,在缺氧、应激或某些病理条件下,eIF4E活性下降,cap依赖性翻译受到抑制,限制了mRNA疗法在肿瘤、神经退行性疾病等复杂环境中的应用。
近日,来自牛津大学的研究团队在Nature Communications发表重要成果,报道了一种增强线性无帽mRNA翻译效率的新方法。业内普遍认为,这项成果将成为2026上海生物医药合作大会关注的焦点之一。

图片来源:RNAScript
研究团队设计了一种含叠氮基的双核苷酸引物 CleaN3,可在体外转录阶段直接引入mRNA的5′端。该结构兼具CleanCap的高引物效率,又为后续的“点击化学”反应提供结合位点。通过与炔基荧光分子AF647进行无铜环加成反应(SPAAC),研究者能在37 °C条件下1小时内完成5′端修饰,产率高达54%,过程简洁且无须复杂纯化。这一方法显著提升了CIT(cap-independent translation)mRNA的稳定性与翻译效率,同时降低了免疫原性。
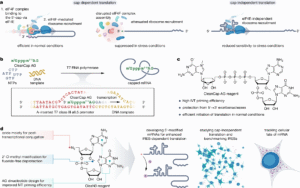
图片来源:RNAScript
为了验证CleaN3策略的有效性,研究者以携带丙型肝炎病毒IRES(HCV IRES)的EGFP报告基因为模型,系统评估了CleaN3及AF647修饰后mRNA的功能表现。结果显示,修饰后的CIT mRNA翻译效率较5′-三磷酸版本提升7.6倍,稳定性提升约1.4倍,并未显著诱导干扰素或促炎因子的释放,其免疫反应水平与商业化有帽mRNA相当。
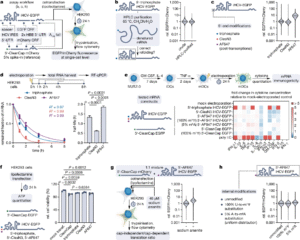
图片来源:RNAScript
更令人关注的是,在细胞应激环境下(如砷酸盐诱导的翻译抑制),5′-AF647 CIT mRNA的翻译活性仍高出有帽mRNA约2.6倍,展现出极强的抗压特性。该体系与当前主流mRNA修饰(m¹Ψ、m⁶A)兼容,并能与之叠加提高效率。研究进一步显示,带AF647修饰的线性无帽mRNA其翻译水平已接近环状RNA(circRNA),说明合理化学设计可弥补cap依赖缺陷。
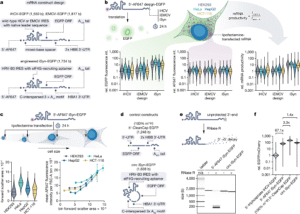
图片来源:RNAScript
此外,该研究的一大亮点是实时荧光追踪。利用AF647标记,研究团队首次完整记录了mRNA从细胞摄取、扩散、聚集、翻译到降解的全过程。结果显示,mRNA进入细胞后会形成多个亚微米级颗粒,主要分布在内质网与溶酶体附近,并在细胞分裂时平均分配给子代细胞。这一“可视化mRNA命运”的手段,为后续研究mRNA药物递送机制及安全性提供了强大工具。
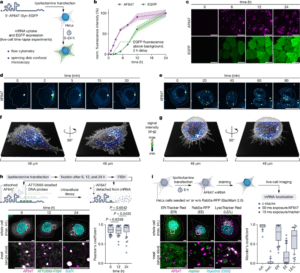
图片来源:RNAScript
综上,CleaN3体系通过引物化学与点击修饰双重创新,为cap-independent mRNA平台提供了全新设计思路。该方法不仅提高翻译效率、降低免疫风险,还可实现荧光追踪和定量化分析。
随着mRNA药物从疫苗向肿瘤免疫与蛋白替代疗法拓展,这项成果有望成为2026上海生物医药合作大会上,学术界与产业界共同探讨的技术亮点之一,为未来国际合作奠定新基础。
文章来源:RNAScript


