CAR-T细胞疗法在血液肿瘤治疗领域取得了突破性进展,但依然面临多方面的临床挑战。生物医药管线CGT合作大会关注到,从实体瘤治疗困境到治疗相关毒性,从生产成本控制到耐药性问题,行业正通过多种创新设计策略寻求解决方案,推动这一革命性疗法向更安全、更有效、更可及的方向发展。
一、 当前临床治疗面临的三大挑战
实体瘤治疗效果有限是CAR-T疗法面临的最严峻挑战。实体肿瘤微环境通过多种机制抑制CAR-T细胞功能,包括物理屏障、免疫抑制细胞浸润、免疫检查点分子高表达等。临床数据显示,CAR-T在实体瘤中的客观缓解率仅为10%-30%,远低于血液肿瘤的60%-80%。肿瘤异质性导致抗原逃逸,单一靶点的CAR-T难以清除全部肿瘤细胞。缺氧、酸性的微环境加速CAR-T细胞耗竭,缩短其在体内的存活时间。
治疗相关毒性仍需优化。细胞因子释放综合征(CRS)和免疫效应细胞相关神经毒性综合征(ICANS)仍然是CAR-T治疗的主要安全顾虑。严重CRS发生率在5%-20%之间,需要ICU监护的患者占比约2%-5%。毒性反应与肿瘤负荷、CAR-T剂量、共刺激结构域选择等因素密切相关。尽管托珠单抗等药物改善了CRS管理,但如何从源头上降低毒性仍是关键课题。治疗相关死亡率约1%-3%,主要集中在老年、高危患者群体。
生产成本与可及性困境。自体CAR-T的个性化制备流程复杂,单个患者治疗成本高达30-50万美元。制备周期长达2-4周,部分患者在等待期间疾病进展。制备失败率约5%-10%,进一步增加治疗成本。医保覆盖有限,全球范围内能够接受治疗的患者比例不足5%。冷链运输、质量控制和规模化生产等技术瓶颈也限制了疗法的普及。
二、 下一代CAR-T的创新设计策略
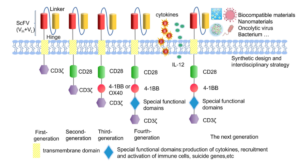
智能化CAR设计提升精准性。逻辑门控CAR系统通过“与”“或”“非”逻辑控制CAR-T激活,仅在多个肿瘤抗原同时存在时才启动杀伤,提高靶向特异性。抑制性CAR(iCAR)表达抑制性受体,在识别正常组织抗原时主动抑制CAR-T功能。可切换CAR通过小分子药物控制CAR-T活性,实现治疗的可逆调控。这些设计有望将脱靶毒性降低一个数量级。
武装化CAR增强抗肿瘤能力。细胞因子装甲CAR表达IL-7、IL-15、IL-21等细胞因子,增强CAR-T扩增和持久性。趋化因子受体装甲帮助CAR-T迁移至肿瘤部位,实体瘤浸润效率提高3-5倍。检查点抑制剂抗体分泌型CAR同时攻击肿瘤和解除免疫抑制。酶催化CAR在肿瘤局部激活前药,实现联合治疗效果。这些武装化策略可使实体瘤缓解率提升至40%-50%。
通用型CAR-T突破制备瓶颈。通过基因编辑技术敲除T细胞的TCR和HLA,降低移植物抗宿主病风险。同时敲除免疫检查点分子,增强抗肿瘤活性。使用病毒特异性T细胞或γδ T细胞等特殊T细胞亚群,提高安全性和疗效。通用型CAR-T制备周期缩短至2-3天,成本降低60%-80%,已进入临床试验阶段,初步数据显示完全缓解率与自体CAR-T相当。
新型CAR结构拓展功能边界。双特异性CAR同时靶向两个肿瘤抗原,减少抗原逃逸。串联CAR(TanCAR)增强对低抗原密度肿瘤的识别敏感性。分泌型CAR局部释放治疗性蛋白,改变肿瘤微环境。可溶性CAR作为“诱饵受体”中和免疫抑制因子。这些新型结构正在临床前研究中展现出突破传统CAR局限的潜力。
三、 关键技术突破方向
基因编辑技术精准调控。CRISPR/Cas9等基因编辑工具实现CAR的精准插入和多基因同时编辑。非病毒载体系统提高转染效率,降低致瘤风险。表观遗传编辑延长CAR-T记忆表型,提高持久性。基因编辑安全性的持续改进是技术突破的关键。
肿瘤微环境重塑策略。联合使用PD-1/PD-L1抑制剂、IDO抑制剂、TGF-β抑制剂等解除免疫抑制。局部放疗或化疗改变肿瘤血管和基质,增强CAR-T浸润。溶瘤病毒与CAR-T联合,发挥协同抗肿瘤效应。这些联合策略正在临床试验中验证。
细胞制造工艺革新。自动化封闭式生产系统提高制备效率和一致性。无血清培养基降低生产成本。低温保存技术延长细胞产品保质期。过程分析技术实现实时质量控制。工艺革新有望将制备失败率降至1%以下。
生物信息学驱动设计优化。单细胞测序分析CAR-T分化状态,指导体外培养工艺。计算模型预测CAR结构和功能关系,加速最佳设计筛选。人工智能算法优化联合治疗方案。数据驱动的方法正在改变CAR-T研发范式。
图片来源:循证拾光
四、 临床应用拓展前景
实体瘤治疗突破可期。针对胶质母细胞瘤、胰腺癌、卵巢癌等实体瘤的CAR-T临床试验已超过200项。多靶点联合、局部给药、预处理方案优化等策略正在提高疗效。未来3-5年,CAR-T在实体瘤中的缓解率有望提升至40%-60%。
适应症向非肿瘤领域扩展。CAR-T在自身免疫病、感染性疾病、纤维化疾病等领域展现出潜力。靶向B细胞的CAR-T治疗系统性红斑狼疮已进入临床研究。靶向HIV感染细胞的CAR-T正在开发中。这些扩展为CAR-T平台技术打开新的市场空间。
治疗关口逐步前移。从末线治疗向一线、巩固治疗甚至预防性治疗推进。CAR-T与造血干细胞移植联合,提高血液肿瘤治愈率。在新诊断患者中,CAR-T可能取代传统化疗成为标准治疗。治疗关口前移将显著扩大适用患者人群。
联合疗法成为主流。CAR-T与双特异性抗体、小分子靶向药、免疫调节剂等联合使用,发挥协同效应。序贯治疗策略优化不同疗法的组合和时机。个体化联合方案基于生物标志物精准选择。联合治疗将CAR-T疗效提升到新的高度。
五、 产业发展趋势展望
技术平台多元化发展。除传统CAR结构外,TCR-T、CAR-NK、CAR-M等新技术平台快速发展。不同技术平台针对不同适应症和患者群体,形成互补格局。平台技术的多元化推动整个细胞治疗领域创新。
生产模式向自动化转型。从人工操作为主向全自动封闭式生产转变。模块化生产单元支持灵活产能配置。分布式生产网络缩短物流距离。生产模式的升级将支撑CAR-T疗法的规模化应用。
支付模式不断创新。疗效挂钩的支付方案分担治疗风险。分期付款降低患者初始负担。商业保险产品专门覆盖细胞治疗。医保谈判推动价格合理化。支付创新提高疗法的可及性。
监管科学同步发展。适应细胞治疗特点的审评标准不断完善。真实世界数据支持监管决策。国际监管协调加速全球开发。监管科学的发展为创新疗法上市提供清晰路径。
CAR-T细胞疗法正处于从血液肿瘤向实体瘤、从末线治疗向前线治疗、从个性化向通用型发展的关键阶段。通过技术创新、工艺优化、临床策略升级,CAR-T有望克服当前困境,成为更广泛癌症患者的标准治疗选择。生物医药管线CGT合作大会认为,这一进程需要学术界、产业界、监管机构的紧密合作,需要长期投入和持续创新,最终实现CAR-T疗法的全部潜力,为癌症治疗带来革命性变革。从突破性技术到主流疗法,CAR-T正在书写肿瘤免疫治疗的新篇章,为无数患者带来新的希望。
文章来源:循证拾光

