引言
随着生物医药技术的飞速发展,mRNA技术在肿瘤免疫治疗领域展现出了巨大的潜力。然而,现有的mRNA-LNP癌症疫苗在诱导高质量肿瘤特异性CD8+T细胞方面仍显不足。为了解决这一难题,研究人员开发了编码膜型IL12(mtIL12)佐剂的新一代mRNA-LNP疫苗,为肿瘤免疫治疗带来了新的突破。

图片来源:清华基础医学院公众号
mRNA肿瘤疫苗的现状与挑战
生物医药产业大会了解到,mRNA肿瘤疫苗通过向体内递送编码肿瘤抗原的mRNA,诱导机体产生针对肿瘤细胞的特异性免疫反应。然而,现有的mRNA-LNP递送体系主要诱导IL-1β、IL-6和IFN-I等细胞因子,虽然能增强抗原特异性CD4+滤泡辅助性T细胞(Tfh)和B细胞反应,但IL-6等细胞因子可能抑制初始T细胞向效应T细胞的分化,从而影响抗肿瘤免疫应答的效果。
图片来源:清华基础医学院公众号
膜型IL-12佐剂的创新设计
为了提升mRNA肿瘤疫苗的疗效与安全性,清华大学基础医学院傅阳心/梁永团队开发了编码膜型IL12(mtIL12)佐剂的新一代mRNA-LNP疫苗。该设计将mtIL12限制性表达在抗原呈递细胞表面,从而在诱导强效肿瘤特异性T细胞应答的同时,有效规避了传统IL-12带来的全身性副作用。
膜型IL-12的构建
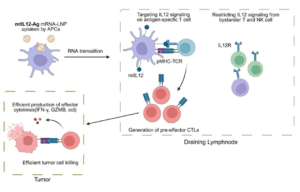
研究团队首先测试了多种作用于CD8+T细胞的强效因子,最终确定IL-12可显著提升mRNA疫苗的抗肿瘤免疫反应。然而,加入分泌型游离IL12(sIL12)编码序列虽然能增强抗肿瘤效果,但也大幅增加了疫苗的全身毒性。为此,团队对IL12编码序列进行改造,在其C端连接跨膜结构域,成功将IL12锚定于被mRNA转染的抗原呈递细胞表面,形成了膜型IL12(mtIL12)。
图片来源:清华基础医学院公众号
mtIL-12疫苗的作用机制
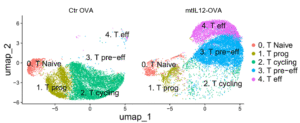
研究团队深入探索了mtIL12疫苗的作用机制。通过细胞删除实验,他们发现mtIL12疫苗的抗肿瘤作用主要依赖于CD8+T细胞。进一步的分析显示,注射mtIL12疫苗的引流淋巴结内产生了一群独特的前效应T细胞(pre-effector T cell),这些细胞是产生外迁性效应T细胞的源泉,具有更强的肿瘤杀伤能力。
临床试验与效果验证
研究团队在多种肿瘤模型中评估了mtIL12佐剂mRNA疫苗的抗肿瘤效力。在所有测试模型中,添加mtIL12佐剂均能产生更强大的抗肿瘤效果,并在外周诱导出效应功能更强的抗原特异性T细胞。这些结果表明,mtIL12佐剂mRNA疫苗不仅显著增强了传统mRNA疫苗的抗肿瘤效应,还大幅降低了IL12的系统毒性。
临床转化价值与未来展望
该研究的核心创新点在于确立了IL12是增强肿瘤mRNA疫苗疗效的有效因子,并通过创新性设计膜型IL12(mtIL12)作为mRNA疫苗佐剂,为优化mRNA肿瘤疫苗提供了新思路。此外,该设计在多种肿瘤模型及临床相关肿瘤抗原靶点中验证了有效性,展现出重要的临床转化价值。
未来,随着对mtIL12佐剂mRNA疫苗研究的深入,生物医药产业大会有望看到这一创新技术在肿瘤免疫治疗领域的广泛应用。同时,这也将进一步推动生物医药技术的发展,为人类健康事业作出更大的贡献。
文章来源:清华基础医学院公众号


