G蛋白偶联受体(GPCR)作为最大的一类药物靶点家族,在人类基因组中超过800个成员,目前已有超过30%的上市小分子药物作用于GPCR靶点。随着结构生物学、计算化学和药物筛选技术的突破,GPCR药物研发正从传统配体结合口袋向变构调节、偏向性信号转导、受体寡聚化等多维度拓展,催生了一系列创新疗法,覆盖神经精神疾病、代谢紊乱、免疫炎症、肿瘤等多个治疗领域。下面2026生物医药产业合作大会就来聊一聊GPCR药物研发:新靶点拓展、多模式创新与适应症突破。
一、 新靶点识别与结构解析突破
孤儿GPCR的功能解码加速靶点验证。随着功能基因组学和反向药理学的发展,大量孤儿GPCR的生理功能和病理相关性被阐明。GPR75被确认为肥胖相关受体,其拮抗剂在临床前研究中可减轻体重、改善糖代谢。GPR52作为精神分裂症的潜在靶点,其调节剂可改善阳性症状和认知障碍。针对这些新靶点的药物已有多个进入临床研究阶段,为疾病治疗提供新选择。
冷冻电镜(Cryo-EM)技术实现高分辨率结构解析。近年来,GPCR-配体-信号蛋白复合物的高分辨率结构不断被解析,揭示了受体激活、信号转导的分子细节。例如,GLP-1R与激动剂和G蛋白复合物的结构解析,指导了长效、高选择性GLP-1类似物的设计。μ阿片受体的结构研究帮助开发镇痛效果强、成瘾性低的新型镇痛药。这些结构信息为基于结构的药物设计(SBDD)提供了坚实基础。
计算预测与人工智能加速靶点-配体匹配。通过机器学习算法分析GPCR序列、结构和功能数据,预测受体与配体的相互作用模式。深度神经网络模型可生成具有理想药代动力学特性的新型配体。虚拟筛选平台可快速评估数百万化合物与靶点的结合潜力,将先导化合物发现时间缩短60%以上。这些技术突破显著提高了靶点验证和药物发现的效率。
二、 信号转导机制的精细调控
偏向性配体实现信号通路的精准调控。传统GPCR激动剂同时激活G蛋白和β-arrestin通路,可能引起不良反应。偏向性配体选择性激活特定信号通路,提高治疗指数。例如,偏向性μ阿片受体激动剂可产生强效镇痛作用,同时减少呼吸抑制和便秘等副作用。β1肾上腺素能受体的偏向性激动剂可增强心脏收缩力,而不引起心律失常。这种精准调控策略正在多个靶点中探索应用。
变构调节剂提供新的调控维度。变构调节剂结合在受体不同于正位结合口袋的位置,可增强或抑制内源性配体的效应。这类分子通常具有更高的受体亚型选择性。代谢型谷氨酸受体5(mGluR5)的负向变构调节剂正在开发用于脆性X综合征、帕金森病等神经系统疾病。GABAB受体的正向变构调节剂可能成为焦虑、抑郁的治疗新选择。变构调节扩展了GPCR的药理学调控空间。
受体寡聚化成为新的调控靶点。GPCR可在细胞膜上形成同源或异源二聚体、多聚体,表现出独特的药理特性。多巴胺D2受体与5-HT2A受体的异源二聚体与精神分裂症相关,针对该复合物的药物可能提供新治疗策略。阿片受体与趋化因子受体的异源二聚体调节疼痛和免疫反应,成为开发非成瘾性镇痛药的潜在靶点。针对受体复合物的药物设计成为新兴研究方向。
三、 新适应症的开拓与临床进展
代谢性疾病治疗不断突破。GLP-1受体激动剂已从糖尿病治疗扩展到肥胖、非酒精性脂肪性肝炎(NASH)、心血管疾病等多个适应症。新一代GLP-1/GIP/胰高血糖素受体多靶点激动剂在临床试验中显示出更优的减重和降糖效果。GPR40激动剂通过促进胰岛素分泌治疗2型糖尿病,已有药物进入III期临床。GPR119激动剂调节肠促胰岛素分泌,可能成为糖尿病治疗新选择。
神经精神疾病治疗迎来新希望。5-HT1A受体部分激动剂治疗焦虑和抑郁已有多年应用,新型高选择性配体正在开发中。靶向D1受体的正性变构调节剂改善精神分裂症的阴性症状和认知障碍。组胺H3受体拮抗剂提高觉醒和认知功能,用于治疗发作性睡病和阿尔茨海默病。这些新靶点药物有望解决现有治疗方案的不足。
免疫炎症性疾病治疗取得进展。趋化因子受体如CCR2、CCR5、CXCR4等的拮抗剂调节免疫细胞迁移,治疗类风湿关节炎、多发性硬化症、炎症性肠病等。前列腺素E2受体EP4的拮抗剂减少炎症反应,可能成为骨关节炎的治疗选择。靶向GPCR的抗体药物也进入临床研究,如CCR4抗体治疗T细胞淋巴瘤已获批准。
肿瘤治疗开辟新途径。趋化因子受体CXCR4的拮抗剂抑制肿瘤转移,在血液肿瘤和实体瘤中显示治疗潜力。LPA受体拮抗剂抑制肿瘤生长和转移,正在多种实体瘤中评估。一些GPCR可作为肿瘤特异性抗原,成为抗体药物偶联物(ADC)或CAR-T疗法的靶点。这些应用扩展了GPCR在肿瘤治疗中的价值。
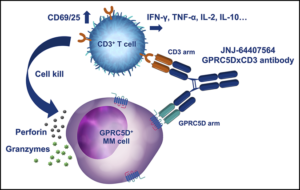
图片来源:小药说药
四、 药物研发技术平台创新
DNA编码化合物库加速苗头化合物发现。通过合成包含数十亿成员的DNA编码化合物库,可一次性筛选大量分子与GPCR的相互作用。这项技术将筛选通量提高1000倍以上,成本降低90%。已有多个通过该技术发现的GPCR配体进入临床研究,证明了平台的有效性。
类器官与器官芯片提高临床前预测性。使用患者来源的类器官或器官芯片模型评估GPCR药物效果,可更好地模拟人体生理和病理状态。肠类器官评估GPCR调节剂对肠内分泌细胞和肠神经的作用。大脑类器官研究神经精神药物对神经网络的影响。这些模型提高了临床前研究的预测性,减少后期失败风险。
基因编辑与疾病模型验证靶点功能。CRISPR/Cas9技术构建GPCR基因敲除或点突变的细胞和动物模型,验证靶点的生理病理功能。人源化动物模型评估药物在人体内的代谢和效应。这些模型为靶点验证和药物评价提供了重要工具,加速研发进程。
生物制剂与细胞疗法拓展治疗模式。除小分子药物外,GPCR也成为抗体、多肽、核酸药物的靶点。针对GPCR的抗体药物可更特异地调节受体功能。GPCR导向的CAR-T细胞疗法正在血液肿瘤中研究。这些新模式扩展了GPCR靶向治疗的手段。
五、 未来展望与挑战
个性化治疗成为发展方向。基于患者的GPCR基因多态性、表达谱和信号特征,选择最合适的药物和剂量。伴随诊断确定最可能受益的患者群体。这种精准医疗方法可提高治疗成功率,减少不良反应。
多靶点药物提高治疗效果。设计同时调节多个相关GPCR的药物,可能产生协同效应。GPCR与其他类型受体(如激酶、离子通道)的双重调节剂也在开发中。这些多靶点策略可能更有效地干预复杂疾病网络。
新递送系统改善药物特性。长效注射制剂提高患者依从性。靶向递送系统提高药物在目标组织的浓度,减少全身副作用。可激活前药在特定部位释放活性成分,提高治疗精准性。这些递送创新可提高GPCR药物的临床价值。
全球合作加速创新。学术机构、生物技术公司、大型药企加强合作,共享知识和技术。国际多中心临床试验加速证据生成。监管协调促进全球同步开发。这种合作模式将推动GPCR药物研发更快发展。
GPCR药物研发正处于创新活跃期,新靶点、新机制、新适应症的不断突破,为多种难治性疾病提供了新的治疗希望。从结构解析到信号调控,从小分子到生物制剂,从单靶点到多靶点,GPCR药物研发正向着更精准、更有效、更安全的方向发展。随着技术进步和临床经验积累,GPCR将继续作为最重要的药物靶点家族之一,为人类健康事业做出重要贡献。从基础研究到临床转化,从概念验证到产品上市,GPCR药物研发正在开启新的篇章,为患者带来更多治疗选择。
文章来源:小药说药


