随着抗体偶联药物(ADC)技术的迭代,双特异性抗体ADC(双抗ADC)正成为乳腺癌治疗领域的新引擎。这类药物通过同时靶向两个不同抗原或同一抗原的不同表位,显著提升了药物的靶向精准性和抗肿瘤效力,为HER2阳性、三阴性乳腺癌(TNBC)及HR+/HER2-等难治亚型带来了新的希望。下面2026上海生物医药合作大会就来聊一聊双抗ADC重塑乳腺癌治疗从机制创新到临床得突破。
一、 双抗ADC的机制优势与设计逻辑
双靶点协同增强内吞效应。传统单靶点ADC在面对肿瘤异质性时易因抗原丢失而耐药。双抗ADC通过同时结合两个靶点(如HER2/HER3、TROP2/HER3),不仅提高了对肿瘤细胞的结合亲和力,更通过“双锁”机制触发更高效的内吞作用,将更多细胞毒性载荷带入胞内。例如,EGFR×HER3双抗ADC(如BL-B01D1)可同时阻断EGFR和HER3信号通路,在TNBC中显示出强效杀伤能力。
载荷技术升级降低脱靶毒性。新一代双抗ADC采用拓扑异构酶I抑制剂(如Exatecan衍生物)作为载荷,相比传统微管蛋白抑制剂,其旁观者效应适中,对正常组织损伤更小。定点偶联技术(DAR=4)确保了药物抗体比(DAR)的均一性,提高了药代动力学的可预测性。此外,双抗ADC的Fc段常经过工程化改造(如FcγR结合能力降低),进一步减少了抗体依赖性细胞吞噬(ADCP)相关的血小板减少等不良反应。
二、 HER2阳性乳腺癌:新辅助与后线治疗的双重突破
早期新辅助治疗实现高病理缓解率。国产双抗ADC TQB2102(靶向HER2双表位)在II期新辅助研究中展现出显著疗效。入组患者接受4周期治疗后,总体病理完全缓解率(tpCR)达到76.9%,且在不同HER2表达水平(包括低表达)患者中均观察到深度缓解。这一数据提示,双抗ADC有望成为HER2阳性早期乳腺癌新辅助治疗的新标准。
后线治疗克服耐药机制。针对曲妥珠单抗耐药患者,双靶点ADC显示出独特优势。ZW49(靶向HER2双表位)在I期研究中,对既往接受过T-DM1或DS-8201治疗的患者仍能实现客观缓解,中位无进展生存期(PFS)较传统ADC延长约30%。其机制在于双靶点设计避免了因单个表位突变导致的耐药。
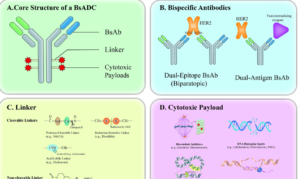
图片来源:小药说药
三、 三阴性乳腺癌(TNBC):突破治疗瓶颈
EGFR×HER3双抗ADC填补治疗空白。TNBC缺乏明确靶点,治疗选择有限。Izalontamab brengitecan(BL-B01D1)作为全球首个进入III期临床的EGFR×HER3双抗ADC,在TNBC后线治疗中表现出色。BL-B01D1-307研究显示,相比研究者选择的化疗(ICC),该药显著延长中位PFS(5.8个月 vs 3.4个月)和总生存期(OS),且安全性可控,口腔炎和血液学毒性发生率低于同类单靶点ADC。
TROP2双靶点ADC提升疗效天花板。针对TROP2高表达的TNBC,双抗ADC通过增加靶点结合密度,提升了药物在肿瘤组织的富集。JSKN016(TROP2/HER3双抗ADC)在I期研究中,对转移性TNBC患者的客观缓解率(ORR)达到45%,且脑转移患者中也观察到颅内病灶缩小,提示其潜在的血脑屏障穿透能力。
四、 HR+/HER2-乳腺癌:内分泌耐药后的新选择
联合SERD打破耐药困局。HR+/HER2-乳腺癌患者在CDK4/6抑制剂耐药后,化疗疗效有限。双抗ADC联合口服选择性雌激素受体降解剂(SERD)成为新策略。JSKN016联合D-0502(口服SERD)的Ib/II期研究显示,联合方案的中位PFS达到9.2个月,显著优于单药化疗的4.5个月,且耐受性良好,未出现新的安全性信号。
精准覆盖HER2低表达人群。双抗ADC凭借其高亲和力,对HER2低表达(IHC 1+或2+/ISH-)肿瘤的识别能力优于传统单抗。TQB2102在HR+/HER2低表达队列中,疾病控制率(DCR)超过80%,为这部分传统上难以从HER2靶向治疗中获益的患者提供了精准治疗选择。
五、 安全性管理与未来方向
毒性谱差异化。双抗ADC的毒性特征与传统ADC有所不同。由于双靶点设计降低了正常组织的非特异性结合,间质性肺病(ILD)的发生率普遍低于单靶点ADC(如DS-8201)。主要不良反应为血液学毒性(中性粒细胞减少、血小板减少)和胃肠道反应(恶心、腹泻),且多为1-2级,通过剂量调整和支持治疗可有效管理。
未来发展方向。双抗ADC正朝着“智能化”方向发展:可裂解连接子设计实现肿瘤微环境特异性释放载荷;双靶点协同阻断信号通路(如HER2+CD63)可抑制耐药克隆产生;联合免疫治疗(双抗ADC+PD-1/PD-L1抑制剂)在TNBC中显示出协同激活T细胞的潜力。随着更多III期临床数据的公布,双抗ADC有望在2026-2027年成为多个乳腺癌亚型的标准治疗组成部分。
从机制创新到临床验证,双抗ADC正在重塑乳腺癌的治疗格局。通过双靶点精准识别、载荷技术升级和联合策略优化,这类药物为不同亚型乳腺癌患者提供了更有效、更安全的治疗选择,标志着ADC疗法进入了全新的“双靶时代”。
文章来源:小药说药


