日前,上海生物医药技术大会 注意到,国家药品监督管理局(NMPA)官网于5月21日显示,恒瑞医药自主研发的PD-1单抗卡瑞利珠单抗与小分子多靶点靶向药苹果酸法米替尼联合疗法新增适应症获批,用于治疗既往接受含铂化疗失败的复发或转移性宫颈癌患者。

截图来源:NMPA官网
关键II期研究数据凸显联合治疗优势
此次获批基于一项随机、开放、多中心关键II期临床研究(SHR-1210-II-217)的积极结果。研究显示,与卡瑞利珠单抗单药或研究者选择的化疗方案相比,联合治疗组在多项核心指标中展现显著获益:
无进展生存期(PFS):联合组中位PFS达8.1个月(95% CI:6.2-12.4),显著优于单药组的4.1个月(95% CI:2.1-5.1)和化疗组的2.9个月(95% CI:2.0-6.2);
总生存期(OS):截至2023年9月25日,联合组中位OS为20.6个月,较单药组(14.9个月)和化疗组(13.9个月)显著延长;
客观缓解率(ORR):联合组经独立评审委员会(BICR)评估的ORR为41%,其中鳞癌亚组达46.9%,非鳞癌亚组为29.2%,且无论PD-L1表达阳性(44.6%)或阴性(40.0%)亚组均观察到缓解。
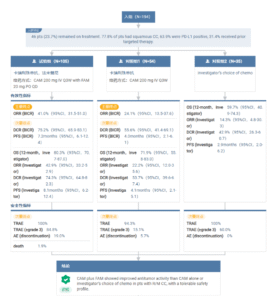
截图来源:Insight 数据库
安全性方面,联合治疗组常见治疗相关不良事件(TRAEs)包括白细胞计数下降、中性粒细胞计数下降、贫血及蛋白尿等,未发现新的安全信号。
药物背景与临床布局
卡瑞利珠单抗是恒瑞医药研发的人源化PD-1单克隆抗体,此前已在国内获批9项适应症,覆盖肺癌、肝癌、食管癌等多个癌种,其中5项为一线治疗。此次宫颈癌适应症是其第10项上市批准。

截图来源:Insight 数据库
法米替尼为恒瑞自主研发的多靶点酪氨酸激酶抑制剂,通过抑制血管生成相关靶点发挥抗肿瘤作用。目前,两药联合一线治疗复发转移性宫颈癌的III期临床研究(SHR-1210-III-329)正在进行中,若研究成功,该组合有望成为晚期宫颈癌一线治疗首个去化疗方案,为患者提供新治疗选择。
宫颈癌治疗现状与市场格局
宫颈癌是我国女性生殖系统发病率最高的恶性肿瘤,复发或转移性患者预后较差,一线治疗失败后治疗选择有限,中位OS仅8-13个月,5年生存率不足15%。近年来,NMPA陆续批准多款PD-1/PD-L1单药及双抗疗法用于宫颈癌二线治疗,如恩朗苏拜单抗、赛帕利单抗、卡度尼利单抗等。2024年9月,齐鲁制药的艾帕洛利托沃瑞利单抗组合疗法也获批准,而恒瑞此次获批进一步丰富了临床治疗选择。

截图来源:Insight 数据库


