近日,生物医药产业大会关注到,肿瘤免疫疗法虽已取得重大进展,但如何让对现有治疗无应答的“冷肿瘤”转化为可被免疫系统识别的“热肿瘤”,仍是领域内核心挑战。近期,一项发表于《自然》的研究带来了突破性思路。北京大学与深圳湾实验室的联合团队通过融合膜蛋白靶向降解与抗原呈递技术,成功开发出一种新型“瘤内疫苗”策略,为克服实体瘤免疫治疗耐药提供了全新方案。
应对临床瓶颈:超60%患者仍面临免疫疗法无效困境
以PD-1/PD-L1抗体为代表的免疫检查点抑制剂,通过解除T细胞抑制来发挥抗肿瘤作用。然而临床数据显示,在非小细胞肺癌等癌种中,仍有超过60%的患者对现有免疫疗法不应答。其关键在于肿瘤细胞常通过下调抗原呈递机制实现免疫隐身,导致肿瘤微环境中缺乏能特异性识别癌细胞的T细胞。
技术融合创新:从降解膜蛋白到“重编程”肿瘤细胞
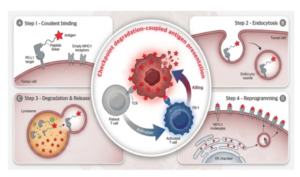
该研究的核心在于将膜蛋白靶向降解技术与抗原呈递过程在肿瘤细胞内进行耦合。团队基于此前开发的GlueTAC平台——一种能特异性降解PD-L1等膜蛋白的“胶水抗体”技术,进一步设计出了一种双功能嵌合分子:瘤内疫苗嵌合体。
文章来源:北京大学化学与分子工程学院
该分子仅18 kDa,具备良好的肿瘤组织渗透能力,由三部分构成:靶向PD-L1的共价纳米抗体、诱导内吞的降解模块、以及可释放抗原的免疫肽段。其作用机制类似于一场细胞层面的“特洛伊木马”行动:分子进入肿瘤细胞后,在降解免疫检查点蛋白的同时,迫使癌细胞摄取并呈递外源抗原,从而将其“重编程”为具有类似抗原呈递细胞功能的免疫激活者。
唤醒沉睡免疫力:调用抗病毒记忆T细胞攻击肿瘤
研究团队选择了具有广泛人群基础的巨细胞病毒(CMV)抗原作为模型。全球超过80%的成年人曾感染CMV,体内存在大量针对该病毒的记忆T细胞,但这些细胞通常处于旁观状态,不识别肿瘤。
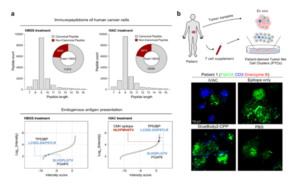
负载CMV抗原的iVAC分子能在肿瘤原位精准激活这些记忆T细胞,将其转化为攻击肿瘤的“战士”。实验表明,经iVAC处理的癌细胞能高效激活抗原特异性CD8⁺ T细胞,效果与专业的树突状细胞相当。在移植了人类肿瘤的小鼠模型中,iVAC疗法展现出比单独使用免疫检查点抑制剂更强的肿瘤抑制效果。
文章来源:北京大学化学与分子工程学院
临床转化潜力:在患者来源类器官中验证可行性
生物医药产业大会了解到,研究进一步在临床病人来源的肿瘤类器官中验证了该策略的可行性。iVAC成功激活了多位不同癌症患者体内预存的CMV特异性T细胞,并实现了对自体肿瘤的有效杀伤。这一结果为其后续临床转化提供了有力支持。
据生物医药产业大会了解,当前蛋白质靶向降解领域正从胞内蛋白向膜蛋白和胞外蛋白快速拓展。此项工作通过降解+免疫的跨领域融合,不仅拓展了靶向降解技术的应用维度,也为开发更具普适性的癌症疫苗提供了全新范式。研究团队表示,正在积极推进该技术的临床转化研究,有望为对现有免疫疗法耐药的患者带来新的治疗选择。
文章来源:北京大学化学与分子工程学院


