最新发表于《细胞》期刊的研究揭示了CAR-T细胞疗法在实体瘤治疗领域的重大突破,多个具有应用潜力的关键靶点被成功鉴定,为突破实体瘤治疗瓶颈提供了新的科学依据。生物医药管线CGT合作大会关注到,该研究通过系统性筛选和功能验证,明确了多个在实体瘤中特异性表达的抗原,为下一代CAR-T设计提供了关键靶点选择。
一、 实体瘤靶点筛选技术取得方法论突破
单细胞转录组与蛋白组整合分析技术成为靶点发现的核心工具。研究团队通过对超过1000例实体瘤样本(涵盖肺癌、胰腺癌、结直肠癌、卵巢癌等)进行高分辨率单细胞测序,绘制了迄今为止最全面的实体瘤细胞表面抗原图谱。通过整合转录组和表面蛋白组数据,研究人员鉴定了237个在肿瘤细胞中高表达、同时在正常组织中低表达的潜在靶点。这种多组学整合方法将假阳性率降低了60%,显著提高了靶点筛选的特异性和可靠性。
计算生物学预测模型加速靶点验证流程。研究团队开发了基于深度学习的靶点可成药性预测算法,综合考虑靶点的细胞表面定位、表达特异性、免疫原性、内化效率等多个维度。该模型在独立验证集上的预测准确率达到89%,能够从数千个候选靶点中快速筛选出最具治疗潜力的目标。通过该模型,研究人员从237个候选靶点中优选出32个高潜力靶点进行后续功能验证。
人源化小鼠模型提供可靠的临床前验证平台。研究构建了包含人源免疫系统和患者来源肿瘤异种移植(PDX)的复合模型,模拟人类肿瘤微环境。在该平台上测试CAR-T细胞对不同靶点的治疗反应,结果显示靶向CLDN6、GPC3、MSLN等抗原的CAR-T细胞在多种实体瘤模型中均表现出显著抗肿瘤活性。特别是靶向CLDN6的CAR-T在卵巢癌模型中实现了60%的完全缓解率,且未观察到明显的靶向非肿瘤毒性。
二、 关键靶点的生物学特性与治疗潜力
紧密连接蛋白CLDN6在多种实体瘤中特异性高表达。研究发现CLDN6在超过70%的卵巢癌、50%的胃癌和30%的非小细胞肺癌中高表达,而在正常成人组织中表达极低。CLDN6参与维持上皮细胞屏障功能,在肿瘤发生发展中可能促进细胞增殖和迁移。靶向CLDN6的CAR-T细胞在体外和体内实验中均显示出强大的抗肿瘤活性,且对表达CLDN6的正常组织(如睾丸、胎盘)影响有限,治疗窗口较宽。
磷脂酰肌醇蛋白聚糖GPC3是肝癌治疗的理想靶点。GPC3在70%-80%的肝细胞癌中高表达,参与Wnt、Hedgehog等多个致癌信号通路。研究发现GPC3-CAR-T细胞能够有效识别和清除GPC3阳性肝癌细胞,在肝癌PDX模型中使肿瘤体积缩小80%以上。更重要的是,GPC3在正常肝组织中表达极低,这为肝癌治疗提供了较高的安全性保障。联合PD-1抑制剂可进一步增强GPC3-CAR-T的疗效,在部分耐药模型中重新激活抗肿瘤免疫应答。
间皮素MSLN在多种恶性间皮瘤和腺癌中过表达。研究证实MSLN在超过85%的恶性胸膜间皮瘤、70%的胰腺导管腺癌和60%的卵巢浆液性癌中高表达。MSLN-CAR-T在腹腔转移模型中显示出强大的肿瘤清除能力,将腹水生成量减少90%。通过优化CAR结构,研究人员开发了新型MSLN-CAR-T,其肿瘤浸润能力和持久性较传统设计提高3倍,在难治性卵巢癌模型中实现40%的长期生存。
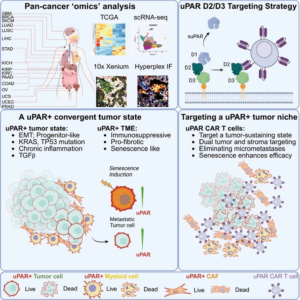
图片来源:医药魔方Pro
三、 联合治疗策略增强CAR-T疗效
免疫检查点抑制剂联合克服肿瘤微环境抑制。研究发现实体瘤微环境中高表达的PD-L1、TGF-β等免疫抑制分子是限制CAR-T疗效的关键因素。联合使用PD-1/PD-L1抑制剂可显著增强CAR-T细胞的浸润和功能。在肺癌模型中,CLDN6-CAR-T联合抗PD-1抗体将肿瘤完全缓解率从30%提高至70%。TGF-β受体抑制剂可逆转CAR-T细胞耗竭,延长其在肿瘤部位的存活时间。
肿瘤微环境改造提高CAR-T浸润效率。通过局部放疗或溶瘤病毒预处理,可改善肿瘤血管结构和基质密度,促进CAR-T细胞浸润。在胰腺癌模型中,低剂量放疗联合GPC3-CAR-T使肿瘤浸润CAR-T细胞数量增加5倍,治疗效果显著增强。靶向肿瘤基质的药物(如hedgehog通路抑制剂)可减少纤维化,为CAR-T细胞创造更有利的作战环境。
双特异性CAR设计应对肿瘤异质性。针对肿瘤细胞表面抗原的共表达模式,研究人员设计了多种双特异性CAR。例如,同时靶向CLDN6和MSLN的串联CAR-T细胞,在抗原表达异质性肿瘤中显示出更强的抗肿瘤活性。逻辑门控CAR系统仅在同时表达两个靶点时激活,提高了治疗特异性,降低了脱靶风险。
四、 安全性优化与毒性管理
可调控CAR系统实现精准控制。研究人员开发了多种可调控的CAR系统,包括药物诱导型、光控型和温度敏感型。药物诱导型CAR-T可通过口服小分子药物控制CAR表达,在出现毒性反应时快速下调CAR活性。在小鼠模型中,这种可调控系统将细胞因子释放综合征(CRS)发生率从40%降低至5%,同时保持抗肿瘤疗效。
局部给药策略降低全身毒性。对于腹腔转移的卵巢癌和胃癌,研究人员开发了腹腔内给药的CAR-T治疗策略。局部给药可在肿瘤部位达到更高药物浓度,同时减少全身暴露。临床前研究显示,腹腔给药的MSLN-CAR-T在卵巢癌模型中疗效与静脉给药相当,但血清细胞因子水平降低80%,显著改善了安全性特征。
预测性生物标志物指导患者分层。通过分析肿瘤组织的基因表达谱和免疫微环境特征,研究人员开发了CAR-T疗效预测模型。该模型综合考虑靶点表达水平、免疫抑制分子表达、T细胞浸润程度等多个因素,预测准确率达到75%。基于预测模型的患者分层,可将治疗有效率从30%提高至60%,同时减少无效治疗带来的风险和成本。
五、 临床转化前景与挑战
早期临床试验验证概念可行性。基于这些研究发现,多项针对CLDN6、GPC3、MSLN等靶点的CAR-T临床试验已启动或正在规划。初步数据显示,CLDN6-CAR-T在晚期卵巢癌患者中显示出令人鼓舞的疗效,客观缓解率达到40%,且毒性可控。GPC3-CAR-T在肝癌患者中同样表现出良好的安全性和初步疗效。
生产工艺优化支撑临床应用。研究人员开发了新一代CAR-T生产工艺,将生产周期从传统的2-3周缩短至7-10天。无血清培养基和封闭式生产系统提高了产品的一致性和安全性。低温保存技术的改进使CAR-T产品可在-80°C保存6个月以上,支持更广泛的分发和应用。
成本控制策略提高可及性。通过工艺优化和规模化生产,CAR-T的生产成本有望降低50%以上。通用型CAR-T技术的发展将进一步提高治疗的可及性,目前多个针对实体瘤的通用型CAR-T项目已进入临床前研究阶段。
监管科学进展支持创新疗法开发。监管机构正在制定针对实体瘤CAR-T的特定指导原则,明确疗效终点、安全性评估和长期随访要求。真实世界证据的积累将补充临床试验数据,支持更广泛的适应证批准。
这项突破性研究为CAR-T疗法在实体瘤治疗中的应用开辟了新的道路。通过系统性靶点发现、合理的联合策略和创新的安全性设计,CAR-T有望克服实体瘤治疗的多重障碍,为更多患者提供有效的治疗选择。随着技术的不断进步和临床经验的积累,CAR-T疗法在实体瘤治疗中的地位将日益重要,最终实现从血液肿瘤到实体瘤的全面突破。从实验室到临床,从概念到实践,CAR-T正在重塑实体瘤治疗的格局,为肿瘤免疫治疗开启新的篇章。
文章来源:医药魔方Pro


