抗体-寡核苷酸偶联物(AOC)正成为继ADC(抗体偶联药物)之后最受关注的下一代精准治疗平台。它巧妙地将抗体的靶向导航能力与寡核苷酸(siRNA/ASO)的基因调控功能结合,旨在突破传统核酸药物“只能靶向肝脏”的局限,将治疗触角延伸至肌肉、中枢神经及肿瘤等组织。2026创新药抗体&ADC合作大会关注到,尽管前景广阔,但其从实验室走向临床的转化之路,仍面临递送效率、安全性及生产工艺等多重深水区挑战。
一、 核心价值:打破“肝脏困局”的精准递送
AOC的设计初衷是解决寡核苷酸药物的肝外递送难题。传统GalNAc偶联技术虽在肝脏表现出色,但对肌肉、心脏及中枢神经系统(CNS)的渗透率极低。AOC利用抗体(如靶向转铁蛋白受体TfR1)作为“特洛伊木马”,通过受体介导的内吞作用,将基因药物定向输送至传统疗法难以触及的病灶。
目前,该领域已从概念验证进入临床深耕期。以Avidity Biosciences、Dyne Therapeutics为代表的公司,在杜氏肌营养不良(DMD)、强直性肌营养不良(DM1)等罕见神经肌肉疾病中取得了突破性进展,部分项目已进入III期临床,证明了该平台在提升肌营养不良蛋白表达方面的显著优势。
二、 临床转化的四大“拦路虎”
尽管原理优美,但AOC的分子复杂性使其临床转化面临比传统抗体或小核酸药物更严峻的挑战。
- “最后一公里”难题:内体逃逸效率低下
AOC能顺利进入细胞,但往往“卡”在细胞内体(Endosome)中无法脱身。目前的内体逃逸效率普遍不足1%-2%,这意味着大量药物在细胞内被降解,无法到达细胞质或细胞核发挥功能。这是制约药效的关键瓶颈,也是当前技术攻关的焦点。
- 免疫原性与安全性平衡
AOC是“双刃剑”:抗体和寡核苷酸均可能触发免疫反应。非人源化抗体易产生抗药抗体(ADA),加速药物清除;而某些寡核苷酸序列(如CpG基序)可能过度激活TLR通路,引发细胞因子风暴或全身炎症。如何在增强药效的同时,通过人源化设计、化学修饰(如2′-O-甲基化)降低免疫原性,是扩大治疗窗口的核心。
- 复杂的药代动力学(PK)与脱靶毒性
AOC在体内存在多种形态:完整偶联体、断裂的游离寡核苷酸等。连接子的稳定性至关重要——太稳定则药物无法释放,太不稳定则导致全身性脱靶毒性(如肝毒性)。此外,目前常用的TfR1靶点广泛表达于红细胞前体等非靶组织,易造成药物“误吞”和剂量浪费。
- CMC(化学、制造与控制)工艺壁垒
AOC的生产是抗体工程与核酸化学的跨界融合,工艺复杂度极高。连接子技术和DAR(药物抗体比)控制是两大痛点。非定点偶联会导致产物异质性,影响药效和安全性;而高DAR(>4)易导致分子聚集和快速清除。建立稳定、均一的大规模生产工艺是商业化的前提。
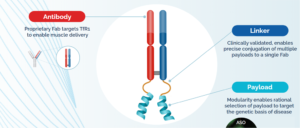
图片来源:小药说药
三、 未来展望:技术迭代与适应症拓展
- 技术平台升级
载体小型化:从全长抗体转向Fab片段、单域抗体(VHH)或环肽,以提升组织穿透力,减少空间位阻。
内体逃逸增强:开发新型环肽或化学增强剂,将逃逸效率从1%提升至更高水平,是决定药效成败的关键。
新靶点挖掘:寻找比TfR1更具组织特异性的新受体,减少非靶向摄取。
- 从罕见病到慢病的市场扩容
目前AOC主攻罕见病(如DMD),但随着递送技术的成熟,其战场将向心血管代谢疾病(如心衰、肥胖)、神经退行性疾病(如阿尔茨海默病)及肿瘤免疫拓展。AOC有望提供季度甚至半年给药一次的长效治疗方案,重塑慢病管理逻辑。
- 监管与产业链协同
随着诺华等巨头百亿美元级的并购入局,AOC领域正加速标准化。建立统一的生物分析标准(特别是PK/PD模型),以及应对长期用药的潜在靶点毒性(如长期占用TfR1)的监管框架,将是产业健康发展的保障。
结语:
AOC正处于从“技术验证”向“临床获益”跨越的关键节点。谁能率先攻克内体逃逸的物理屏障、解决生产工艺的化学难题,谁就能在精准医疗的下一个十年中,掌握基因治疗递送的主导权。
文章来源:小药说药


