上海国际生物医药合作大会关注到,随着基因药物技术的突破性进展,寡核苷酸疗法正成为治疗罕见神经肌肉疾病的关键策略。基于反义寡核苷酸(ASO)和小干扰RNA(siRNA)等技术的特异性分子药物,能够针对疾病相关基因的异常表达进行精准调控,为脊髓性肌萎缩症、杜氏肌营养不良、亨廷顿病等难治性神经系统疾病提供了前所未有的治疗选择。
一、 精准治疗机制的分子基础
反义寡核苷酸(ASO) 通过碱基互补配对原理与目标RNA序列特异性结合,可调节基因表达的多重机制。在DMD治疗中,外显子跳跃ASO能够跳过致病突变所在的外显子,产生截短但仍有部分功能的抗肌萎缩蛋白。诺西那生钠(Spinraza)通过修饰磷酸骨架增强稳定性,在脑脊液中达到治疗浓度,使SMA患者运动功能显著改善。最新一代ASO采用多种化学修饰组合,将组织半衰期从数周延长至数月,降低给药频率。
小干扰RNA(siRNA) 通过RNA干扰机制实现基因沉默,对显性遗传疾病具有特殊价值。针对亨廷顿病致病基因HTT的siRNA药物,在临床试验中可降低突变蛋白水平达50%以上。GalNAc偶联技术将siRNA特异递送至肝细胞,用于治疗遗传性转甲状腺素蛋白淀粉样变性。新型脂质纳米颗粒(LNP)突破血脑屏障限制,使CNS疾病治疗成为可能。
立体化学优化 显著提升治疗效能。硫代磷酸、2′-O-甲氧乙基、锁核酸等化学修饰增强核酸酶抗性,改善药代动力学特性。吗啉代寡聚物(PMO)呈电中性,显著降低免疫原性,在DMD治疗中表现出良好安全性。肽核酸(PNA)具有更强结合亲和力,正在探索性临床试验中验证潜力。
二、 罕见神经肌肉疾病治疗进展
脊髓性肌萎缩症(SMA) 治疗实现突破性进展。三种ASO药物已获FDA批准,通过不同机制增加SMN蛋白表达。利司扑兰(Evrysdi)作为口服小分子,可穿透血脑屏障调节SMN2前mRNA剪接。这些治疗将1型SMA患者2年生存率从不足10%提高至90%以上,实现了从姑息治疗到疾病修饰的转变。
杜氏肌营养不良(DMD) 迎来多靶点治疗时代。针对特定外显子跳跃的ASO药物已批准用于约30%的DMD患者,可将疾病进展延缓数年。微小抗肌萎缩蛋白基因疗法与ASO联合使用,可能产生协同效应。新一代外显子跳跃药物正在开发中,目标是覆盖80%以上DMD患者。
肌萎缩侧索硬化(ALS) 治疗探索取得进展。针对SOD1基因的ASO药物Tofersen在III期临床试验中显著降低脑脊液神经丝轻链水平,延缓疾病进展。针对C9orf72基因六核苷酸重复扩增的ASO药物正在早期临床试验中,可能延缓家族性ALS病程。
亨廷顿病(HD) 迎来疾病修饰希望。多种ASO和siRNA药物正在临床试验中评估降低突变亨廷顿蛋白的能力。TOMINERSEN的II期研究显示剂量依赖性降低突变蛋白水平,但高剂量组出现不良事件。新一代药物正在优化给药方案,平衡疗效与安全性。
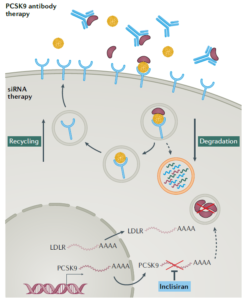
图片来源:Giboy
三、 递送技术突破
CNS递送系统 实现重大进展。鞘内注射直接将药物输送到脑脊液,绕过血脑屏障,已成为SMA标准治疗方案。颅内注射在ALS和HD临床试验中验证可行性。新型LNP通过表面修饰靶向血脑屏障特异性受体,提高脑部药物浓度。外泌体作为天然递送载体,展示出穿越血脑屏障的潜力。
肌肉靶向递送 技术不断优化。全身给药后,经化学修饰的寡核苷酸在骨骼肌和心肌中积累,达到治疗浓度。抗体-寡核苷酸偶联物(AOC)通过靶向肌肉特异性抗原,提高递送效率。细胞穿透肽增强细胞内化,正在临床前研究中验证效果。
口服递送 取得突破性进展。新型纳米载体保护寡核苷酸免受胃肠道降解,促进肠道吸收。利司扑兰的成功证明了口服给药的可行性,为开发更多口服寡核苷酸药物提供了范例。透皮给药、吸入给药等替代途径也在探索中。
四、 临床挑战与应对策略
免疫原性管理 仍是关键课题。未经修饰的寡核苷酸可激活Toll样受体,引发全身炎症反应。通过化学修饰减少免疫刺激基序,降低免疫原性。个体化给药方案,根据患者免疫状态调整剂量。联合使用免疫调节剂,控制炎症反应。
长期安全性 需要持续监测。寡核苷酸可能与非靶标RNA结合,产生脱靶效应。通过全转录组分析评估脱靶风险,优化序列设计。长期动物研究评估潜在毒性,包括肝肾功能、凝血功能、神经系统影响等。建立患者登记系统,收集真实世界安全数据。
治疗成本 影响可及性创新。多数寡核苷酸药物年治疗费用超过10万美元,限制广泛应用。价值导向定价策略,将价格与临床获益挂钩。风险分担协议,支付方与药企共担疗效不确定性。仿制药开发,专利到期后降低价格。
个体化治疗 成为发展方向。基因检测确定患者突变类型,选择最适药物。生物标志物监测治疗反应,指导剂量调整。联合用药策略,针对不同病理机制多靶点干预。基因编辑与寡核苷酸治疗结合,实现长效治愈。
五、 未来展望与技术趋势
新一代化学修饰 提升药物性能。立体定向控制合成单一对映体,提高靶向特异性。新型核苷类似物增强结合亲和力,降低有效剂量。可裂解连接子实现可控释放,延长作用时间。这些进步将改善疗效安全性平衡。
智能递送系统 实现精准定位。刺激响应型纳米颗粒在目标组织特定环境(如pH、酶)下释放药物。双靶向配体同时识别血脑屏障和靶细胞,提高递送效率。基因编码的递送系统利用患者自身细胞产生治疗性寡核苷酸。
联合治疗策略 发挥协同效应。寡核苷酸与小分子药物联合,从多途径干预疾病进程。不同机制寡核苷酸组合,实现多重基因调控。寡核苷酸与基因编辑结合,先调节后修复。这些策略可能产生叠加或协同效应。
疾病预防 成为可能目标。在症状前阶段进行治疗,阻止疾病发生。新生儿筛查识别高风险个体,早期干预。产前治疗在胎儿期纠正基因缺陷。这些方法可能实现疾病的根本性预防。
寡核苷酸疗法正在彻底改变罕见神经肌肉疾病的治疗格局。从单一疾病到多种疾病,从症状管理到疾病修饰,从高副作用到精准靶向,这一领域持续快速发展。随着技术进步和临床经验积累,寡核苷酸疗法将为更多罕见病患者带来希望,推动精准医学向更高水平发展。从实验室到临床,从技术创新到治疗实践,寡核苷酸正在书写神经肌肉疾病治疗的新篇章,为患者提供更有效、更安全的治疗选择。
文章来源:Giboy


