2026创新药抗体&ADC合作大会了解到,最近在免疫衰老与免疫系统重塑研究中,一项发表于《PNAS》的基础研究为免疫细胞来源提供了颠覆性解释。由德国癌症研究中心 Hans-Reimer Rodewald、Thomas Höfer 教授与中国南京医科大学 Xi Wang 教授联合领导的国际团队发现:人体并非仅依赖骨髓造血干细胞(HSC)维持血液系统,而是存在两个长期并行运转的造血系统。其中,绝大多数免疫细胞并非来源于经典造血干细胞通路,而是由一种在胚胎期即形成、并持续存在于成年阶段的胚胎多能前体细胞(embryonic multipotent precursors, eMPPs)产生。

图片来源:生物谷
长期以来,造血领域沿用“单一源头”模型:骨髓中的造血干细胞被视为红细胞、粒细胞和免疫细胞等所有血细胞的起点,再通过多能祖细胞逐级分化成熟。然而,该研究通过高分辨率谱系追踪技术证明,这一模型过于简化,无法解释免疫系统在发育、稳态维持及衰老过程中的关键变化。
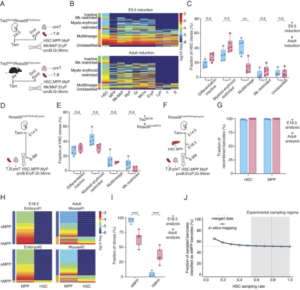
研究团队开发了可在数月尺度内追踪单个血细胞命运的遗传标记体系,对小鼠体内血细胞来源进行系统分析。结果显示,约三分之一的血细胞来自 eMPPs 系统,并且两套造血系统在功能上存在清晰分工:
- eMPPs 系统主要负责生成淋巴细胞等核心免疫细胞,是免疫系统的“主力生产线”
- HSC-hMPP 系统则主要生成红细胞和粒细胞等髓系细胞,承担基础造血任务
更重要的是,eMPPs 并非胚胎发育阶段的短暂产物,而是可长期自我更新,在成年期持续为免疫系统提供关键细胞来源。
图片来源:生物谷
为实现对 eMPPs 的精准识别与功能研究,研究团队进一步开发了名为 PolySMART 的多维单细胞分析技术,可在同一细胞中同时解析 DNA 条形码、表面标记及转录特征。借助这一工具,研究者发现 CD138 是 eMPPs 的关键分子标记。此前,CD138 多被视为多发性骨髓瘤相关标志物,而该研究证明,CD138⁺ 细胞群体正是具有自我更新能力、并天然偏向淋巴系分化的 eMPPs。该发现使 eMPPs 得以被稳定分离和系统研究,标志着造血与免疫发育研究的重要技术突破。
从机制层面看,这一“双引擎”造血模型为免疫衰老提供了清晰解释。研究显示,随着年龄增长,eMPPs 数量逐渐减少,直接导致淋巴细胞生成能力下降,从而引发老年个体免疫应答减弱、感染风险升高等现象。这一结果将“免疫力下降”从功能层面追溯至细胞来源层面,构建了更完整的生物学因果链条。
在应用层面,该研究对创新药、抗体及 ADC 研发具有重要启示意义。免疫细胞来源的重新界定,为免疫缺陷、自身免疫疾病以及肿瘤免疫治疗提供了新的细胞学干预思路。未来,围绕 eMPPs 的激活、保护或定向扩增,有望开发全新的免疫调控策略;而 CD138 作为可操作的分子标记,也为精准靶向提供了现实基础。
研究团队已明确表示,下一阶段将验证人类造血系统中是否同样存在 eMPPs-HSC 两套平行分支。若这一机制在人类中得到确认,将对骨髓移植、细胞治疗以及抗衰老相关药物研发产生深远影响,也将为2026创新药抗体&ADC合作大会所关注的免疫治疗创新提供坚实的基础科学支撑。
文章来源:生物谷


