在抗体药物偶联物(ADC)技术快速发展的同时,一类创新药物形式——抗体-降解剂偶联物(Degrader Antibody Conjugate, DAC)正成为生物医药领域的新焦点。2026创新药抗体&ADC合作大会关注到,这类技术将抗体的靶向递送能力与靶向蛋白质降解(TPD)的高效作用机制相结合,为传统“不可成药”靶点提供了全新的干预策略。
一、 技术原理:抗体递送与靶向降解的协同
DAC的核心设计理念是将具有蛋白质降解功能的分子(如PROTAC、分子胶等)通过连接子与靶向性抗体偶联,利用抗体的特异性将降解剂精准递送至目标细胞或组织,从而实现对靶蛋白的局部、高效降解。
抗体部分提供精准的靶向性。与传统ADC类似,DAC的抗体部分负责识别并结合靶细胞表面的特异性抗原,通过受体介导的内吞作用进入细胞。理想的抗体应具备高亲和力、高内化效率及良好的药代动力学特性。目前研究中多采用人源化或全人源单克隆抗体,以降低免疫原性。
降解剂部分是作用的核心。与ADC的细胞毒性载荷不同,DAC搭载的是可募集E3泛素连接酶并诱导靶蛋白泛素化降解的小分子。这些小分子降解剂通常由两个配体(分别结合靶蛋白和E3连接酶)通过连接子连接而成。它们在极低剂量下即可催化性地诱导蛋白质降解,理论上具有更高的效力和克服耐药性的潜力。
连接子是稳定与释放的关键。连接子需要在血液循环中保持稳定,防止载荷提前释放引起脱靶毒性;同时,在抗体-抗原复合物内吞进入溶酶体后,又需要在酸性或酶促条件下被有效切割,释放出具有活性的降解剂分子。可裂解连接子(如肽键、二硫键)和不可裂解连接子在设计中各有考量。
二、 研发进展:从概念到临床的探索
目前,DAC技术整体处于临床前和早期临床开发阶段,但已展现出令人瞩目的潜力。
临床前概念验证成果频出。多家生物技术公司与学术机构报告了针对不同靶点的DAC分子的临床前数据。例如,有研究报道了靶向HER2的DAC分子,在HER2阳性肿瘤模型中显著降解了胞内的致癌蛋白,并显示出比传统ADC更优的抗肿瘤活性。另有团队开发了靶向B细胞表面CD79b的DAC,成功降解了关键的转录因子,为B细胞淋巴瘤治疗提供了新思路。
技术平台不断优化。为了克服DAC分子在溶解性、稳定性、药代动力学等方面的挑战,研究者们正在优化多个环节。包括开发新型E3连接酶配体以拓展可靶向的E3连接酶库;设计更稳定的连接子-载荷化学;筛选具有更佳内化特性的抗体等。这些优化旨在提高DAC的治疗指数(疗效与毒性的窗口)。
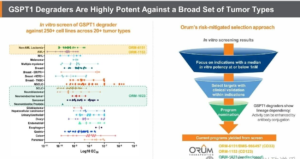
首款候选药物步入临床。2023年,生物技术公司Orum Therapeutics宣布其针对不可成药致癌蛋白KRAS G12D的DAC药物ORM-5029(靶向GPC3)的I期临床试验完成首例患者给药,标志着全球首款DAC药物正式进入人体试验阶段,是DAC技术发展的一个重要里程碑。
图片来源:学以致道乎
三、 核心优势与潜在挑战
核心优势:
拓展靶点空间:有望靶向传统小分子抑制剂和单抗难以作用的“不可成药”靶点,如转录因子、支架蛋白等。
高效催化作用:降解剂以催化模式工作,理论上低于化学计量的药物浓度即可实现持续、深度的靶蛋白清除,效力高,且可能克服因靶蛋白过表达或突变导致的耐药。
高组织选择性:利用抗体的靶向性,可将降解剂局限在特定病变组织,可能提高安全性,减少全身暴露带来的毒性。
潜在挑战:
分子设计与复杂性:构建一个兼具良好抗体药代动力学、高效内化、稳定连接、以及有效释放和功能的降解剂的三元复合物极具挑战,分子量大、理化性质复杂。
“钩状效应”风险:高抗原表达可能导致抗体饱和,影响对低抗原表达细胞的杀伤,即“旁观者效应”可能不如某些ADC显著。
PK/PD关系复杂:降解剂的催化模式、靶蛋白的再合成速率、抗体的内化与降解动力学等因素交织,使得药代动力学/药效学关系复杂,建模和剂量优化困难。
可能的耐药机制:肿瘤细胞可能通过下调抗原表达、改变内吞途径、或突变E3连接酶结合界面等机制产生耐药。
四、 未来展望
DAC代表了将靶向递送与催化降解相结合的下一代精准治疗范式。随着首批临床研究数据的读出,其安全性和初步疗效将得到验证。
未来,该技术的发展将聚焦于:
1)发现和验证更优的靶点-降解剂-抗体组合;
2)深入理解其独特的体内作用机制和潜在耐药性;
3)探索在肿瘤以外的疾病领域(如自身免疫病、纤维化疾病)的应用潜力。
尽管前路充满挑战,DAC技术为攻克难治性疾病开辟了一条充满希望的新途径。
文章来源:学以致道乎


