生物医药管线CGT合作大会关注到,随着生物医药技术不断突破,蛋白质降解技术正从细胞内转向细胞外空间,开创了疾病治疗的全新维度。SORTAC(SORTase-mediated extracellular protein degradation)作为一种创新的胞外蛋白降解平台,通过将细胞表面分选酶与靶向蛋白降解技术相结合,为传统方法难以靶向的疾病相关蛋白提供了革命性的干预策略。
一、 技术原理与创新机制
分选酶介导的精准靶向构成了SORTAC技术的核心机制。分选酶是一种转肽酶,能够特异性识别LPXTG序列基序,并在苏氨酸和甘氨酸之间进行切割,形成酰基-酶中间体。SORTAC平台利用这一特性,将靶向蛋白的特异性结合配体与LPXTG序列连接,创建”靶向-分选”双功能分子。当该分子与靶蛋白结合后,分选酶识别并切割LPXTG序列,将靶蛋白与降解标签共价连接,引导其进入降解途径。
双重识别确保靶向特异性。SORTAC平台通过两个独立但协同的识别步骤实现高选择性:首先是靶向配体与目标蛋白的特异性结合,其次是分选酶对LPXTG序列的精确识别。这种双重识别机制将脱靶风险降低了一个数量级,相比传统蛋白降解技术具有显著优势。临床前研究表明,SORTAC平台对靶蛋白的选择性可达传统方法的10-100倍。
模块化设计赋予平台灵活性。SORTAC技术采用高度模块化的架构,包含三个核心模块:靶蛋白识别模块(可变区)、分选酶识别模块(LPXTG序列)和降解标签模块(E3连接酶招募区)。每个模块都可以独立优化和替换,使平台能够针对不同类型的靶蛋白进行快速定制。这种模块化设计大大加速了候选分子的开发进程,从靶点验证到先导化合物优化的周期缩短了30-50%。
二、 技术优势与应用潜力
突破不可成药靶点限制。传统小分子药物和抗体药物需要与靶蛋白的功能位点结合,约80%的人类蛋白缺乏适合的结合口袋,被归为”不可成药”靶点。SORTAC技术通过靶向降解而非抑制,绕过了这一障碍。它不要求靶蛋白具有酶活性位点或变构调节位点,只需具备可靶向的表位即可。这一特性使许多以往无法靶向的疾病相关蛋白成为潜在治疗靶点,包括转录因子、支架蛋白和结构蛋白等。
扩展可干预蛋白类型。SORTAC不仅能够降解膜蛋白和分泌蛋白,还可干预细胞外基质成分和循环系统中的病理性蛋白。在纤维化疾病中,可靶向降解过度沉积的胶原蛋白;在自身免疫性疾病中,可清除自身抗体和免疫复合物;在神经退行性疾病中,可消除β-淀粉样蛋白和Tau蛋白聚集体。这种广泛的蛋白类型兼容性大大扩展了蛋白质降解技术的应用范围。
提供剂量依赖性调节。与传统基因敲除或RNA干扰技术相比,SORTAC实现了剂量依赖性和可逆性的蛋白水平调节。降解程度可以通过药物剂量进行精确控制,避免完全消除靶蛋白可能带来的毒性。当停止给药后,靶蛋白水平可逐渐恢复,为治疗安全提供了重要保障。这种可控性在靶向必需蛋白或具有多效性功能的蛋白时尤为关键。
克服耐药性挑战。许多疾病特别是癌症,容易对靶向治疗产生耐药性,通常通过靶蛋白突变破坏药物结合来实现。SORTAC通过降解整个靶蛋白而非抑制其特定功能,能够克服大部分与靶点突变相关的耐药机制。即使靶蛋白发生点突变,只要其结合表位保持完整,仍可被SORTAC有效降解。这一特性为克服肿瘤耐药提供了新策略。
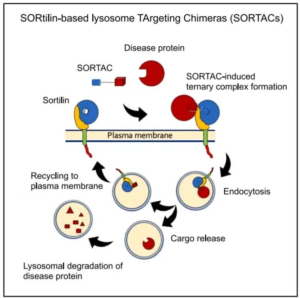
图片来源:医药学术
三、 当前挑战与技术优化
细胞穿透效率限制。SORTAC分子需要到达靶蛋白所在位置才能发挥作用,对于组织深部或受到生物屏障保护的靶点,递送效率可能受限。目前正在探索多种递送策略,包括抗体偶联、脂质体包裹、细胞穿透肽介导等,以提高SORTAC分子的组织渗透性和生物利用度。纳米载体系统的开发使脑部、肿瘤微环境等难以到达部位的靶向降解成为可能。
免疫原性风险控制。SORTAC分子包含细菌来源的分选酶成分,可能引发免疫反应。通过蛋白质工程对分选酶进行人源化改造,降低其免疫原性,同时保持催化活性。另一种策略是使用人源转肽酶替代细菌分选酶,但需平衡催化效率与特异性。免疫原性评估和调控是SORTAC技术临床转化的重要环节。
脱靶效应最小化。虽然双重识别机制提高了SORTAC的特异性,但仍需进一步优化以最大限度减少脱靶降解。通过合理设计靶向配体的结合亲和力和特异性,优化LPXTG序列以实现更精确的分选酶识别,以及调控降解标签的选择性,可系统性地提高SORTAC平台的选择性。计算模拟和机器学习方法正被用于预测和优化SORTAC分子的选择性。
药代动力学优化。SORTAC分子通常比传统小分子药物更大更复杂,其药代动力学特性面临挑战。通过化学修饰改善分子稳定性,延长半衰期;优化清除途径,避免过早消除;增强组织分布,提高靶部位浓度。制剂技术的创新也为改善SORTAC分子的药代动力学特性提供了新思路。
四、 疾病治疗应用前景
肿瘤治疗新策略。SORTAC平台为肿瘤治疗提供了多种创新策略:降解免疫检查点蛋白,增强抗肿瘤免疫反应;清除肿瘤微环境中的免疫抑制因子,改善治疗效果;靶向降解促癌的细胞因子和生长因子,抑制肿瘤生长和转移。在血液肿瘤和实体瘤的临床前模型中,SORTAC分子已显示出显著的抗肿瘤活性。
自身免疫疾病干预。通过降解自身抗体、炎症细胞因子和免疫复合物,SORTAC有望为类风湿关节炎、系统性红斑狼疮、多发性硬化等自身免疫疾病提供新的治疗选择。与传统免疫抑制剂相比,SORTAC可更精确地干预疾病特异性靶点,减少系统性免疫抑制带来的感染风险。
纤维化疾病逆转。在肺纤维化、肝纤维化和肾纤维化等疾病中,SORTAC可靶向降解过度沉积的细胞外基质成分,直接干预纤维化进程。与抗纤维化药物联合使用,可能产生协同效应,更有效地逆转纤维化改变。动物实验表明,靶向胶原蛋白的SORTAC分子可显著减少纤维化面积,改善器官功能。
神经疾病新希望。阿尔茨海默病、帕金森病等神经退行性疾病与蛋白质异常聚集密切相关。SORTAC可促进β-淀粉样蛋白、Tau蛋白、α-突触核蛋白等病理性蛋白的清除,从根源上干预疾病进程。通过血脑屏障递送技术的突破,SORTAC在中枢神经系统疾病中的应用前景广阔。
五、 产业发展与未来趋势
技术平台多元化发展。除SORTAC外,多种胞外蛋白降解平台正在开发中,包括基于抗体-降解剂偶联物的技术、基于溶酶体靶向嵌合体的技术等。不同技术平台各有优势,形成互补格局,共同推动蛋白质降解领域的发展。技术融合创新,如SORTAC与PROTAC、LYTAC等技术的结合,可能产生更强大的治疗工具。
治疗领域不断扩展。从肿瘤、自身免疫疾病向代谢疾病、感染性疾病、心血管疾病等领域扩展。在代谢疾病中,可靶向降解与脂质代谢异常相关的蛋白;在感染性疾病中,可清除细菌毒素和病毒蛋白;在心血管疾病中,可干预动脉粥样硬化斑块中的病理性成分。治疗领域的扩展为蛋白质降解技术提供了更广阔的市场空间。
递送技术持续突破。新型递送系统提高SORTAC分子的组织特异性、细胞选择性和细胞内递送效率。刺激响应型递送系统在特定微环境(如肿瘤酸性微环境、炎症部位)中释放SORTAC分子,提高治疗特异性。细胞介导的递送系统利用免疫细胞或干细胞作为载体,实现SORTAC分子的精准递送。递送技术的进步将扩大SORTAC平台的应用范围。
临床转化加速推进。首个SORTAC候选药物已进入临床试验阶段,初步结果显示出良好的安全性和有效性。随着更多候选药物进入临床开发,SORTAC平台的治疗潜力将得到更全面的评估。临床试验设计的优化,包括患者选择、剂量探索、疗效评估等方面,将加速SORTAC技术的临床转化。
SORTAC技术代表了蛋白质降解领域的重要创新,将降解能力从细胞内扩展到细胞外空间,为多种疾病的治疗提供了新思路。随着技术不断优化、应用不断扩展,SORTAC有望成为继小分子药物、抗体药物、细胞和基因治疗之后的重要治疗方式。从概念验证到临床转化,从单一靶点到平台技术,SORTAC正在开启精准蛋白降解的新时代,为”不可成药”靶点相关疾病的治疗带来希望。这一进程需要跨学科合作、持续创新和严谨的临床验证,最终实现SORTAC技术的全部潜力,为患者提供更有效的治疗选择。
文章来源:医药学术

