在阿尔茨海默病治疗研究领域,科学家们正探索一种突破性的策略——利用SPYTACs(Soluble Protein-Targeting Chimeras)技术实现β-淀粉样蛋白的定向降解。上海国际生物医药合作大会认为,这一创新方法有望克服传统抗体疗法在穿越血脑屏障和清除Aβ聚集物方面的局限性,为神经退行性疾病的治疗开辟全新可能。
一、 血脑屏障穿透:治疗阿尔茨海默病的关键挑战
传统抗体疗法的局限显而易见。尽管靶向Aβ的单克隆抗体在临床试验中显示出部分认知改善效果,但抗体药物通常难以高效通过血脑屏障。数据显示,静脉注射的抗体仅有约0.1%-0.3%能够进入中枢神经系统,导致治疗所需剂量极高,不仅增加治疗成本,还可能引发脑水肿、微出血等副作用。
小分子药物的渗透优势为SPYTACs提供了设计思路。与抗体不同,分子量小于500道尔顿的化合物通常能够较好地穿过血脑屏障。SPYTACs正是利用这一特性,通过巧妙的设计将蛋白质降解机制与血脑屏障穿透能力结合,创造出既能靶向Aβ、又能高效进入中枢神经系统的新型治疗分子。
二、 SPYTACs技术原理:双功能分子的精确作用机制
双功能结构设计实现精准降解。SPYTACs分子包含两个关键功能域:一端是能够特异性结合靶蛋白(如Aβ)的配体,另一端是招募细胞内降解系统(如泛素-蛋白酶体系统)的结构域。这两个功能域通过化学连接子结合,形成分子量通常小于1000道尔顿的小分子药物,兼具血脑屏障穿透能力和蛋白质降解功能。
泛素-蛋白酶体通路介导靶向降解。当SPYTACs分子进入神经元后,其结合域与Aβ蛋白结合,同时招募E3泛素连接酶。E3连接酶将泛素标签标记在Aβ蛋白上,被标记的Aβ随后被蛋白酶体识别并降解。这一过程模拟了细胞内自然发生的蛋白质质量控制机制,但将其重定向至特定的疾病相关蛋白。
化学降解技术的持续优化。最新一代SPYTACs在稳定性和特异性方面取得显著进展。研究人员通过优化连接子长度和化学性质,平衡了分子在血脑屏障穿透、靶点结合和降解效率之间的多重需求。某些候选分子的脑脊液/血浆浓度比可达传统抗体的10倍以上,同时在动物模型中显示出良好的Aβ清除效果。
三、 技术优势:多重机制的协同效应
高效的Aβ清除能力得到实验验证。在小鼠阿尔茨海默病模型中,SPYTACs能够清除超过60%的可溶性Aβ寡聚体和30%的不溶性Aβ斑块,改善幅度显著高于传统抗体治疗。值得注意的是,SPYTACs不仅清除细胞外的Aβ沉积,还能降解细胞内积累的Aβ,这是抗体难以触及的区域。
多靶点协同作用潜力巨大。与传统抗体通常针对单一靶点不同,SPYTACs平台可设计为同时靶向Aβ和tau蛋白等多种致病蛋白。这种多靶点策略有望更全面地干预阿尔茨海默病的病理过程,产生协同治疗效应。初步研究显示,双特异性SPYTACs在动物模型中同时减少淀粉样斑块和神经纤维缠结,改善认知功能的效果优于单一靶点药物。
可控的药代动力学特性提高安全性。SPYTACs的半衰期通常在数小时内,远低于抗体药物的数周,这意味着药物在体内的暴露时间可控,一旦出现不良反应可迅速终止。小分子特性也简化了给药方案,可通过口服或皮下注射给药,显著改善患者的治疗依从性。
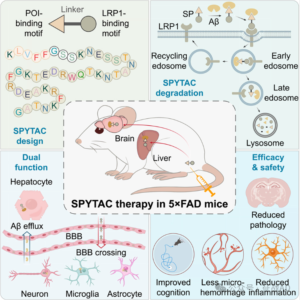
图片来源:征战AD
四、 临床转化前景与挑战
临床前研究进展令人鼓舞。多项独立研究证实,SPYTACs能够显著减少转基因小鼠脑内的Aβ负荷,改善认知功能,且未观察到明显的神经炎症或脑血管损伤。在非人灵长类动物中,SPYTACs也显示出良好的血脑屏障穿透性和Aβ清除能力,为临床试验奠定了基础。
首个人体临床试验正在规划。基于临床前研究的积极结果,至少两家生物技术公司计划在2024-2025年启动SPYTACs治疗阿尔茨海默病的I期临床试验。试验将重点关注药物的安全性、药代动力学和初步疗效信号,特别是对脑脊液和正电子发射断层扫描中Aβ水平的影响。
潜在挑战仍需克服。尽管前景广阔,但SPYTACs仍面临一些科学和转化挑战。脱靶效应是需要重点监测的安全问题,E3连接酶的选择性、SPYTACs对非靶蛋白的可能影响都需严格评估。长期疗效和安全性也需要更长时间的观察,特别是药物对血脑屏障完整性和神经血管单位功能的潜在影响。
个性化治疗成为可能方向。未来SPYTACs治疗可能根据患者的Aβ亚型、疾病阶段和遗传背景进行个性化设计。例如,针对ApoE4携带者或TREM2基因突变患者,可开发特定的SPYTACs变体。治疗监测也将更加精准,通过脑脊液生物标志物和神经影像学评估实时调整治疗方案。
五、 行业影响与未来展望
治疗范式转变的潜在推动力。如果SPYTACs在临床试验中取得成功,可能推动阿尔茨海默病治疗从“症状缓解”向“疾病修饰”的根本转变。与传统的抗淀粉样蛋白疗法相比,SPYTACs提供了更直接、更高效的Aβ清除机制,可能在疾病更早期产生更显著的治疗效果。
技术平台扩展的多重机遇。SPYTACs技术不仅限于阿尔茨海默病,也可应用于其他神经退行性疾病,如帕金森病、亨廷顿病、肌萎缩侧索硬化等。通过更换靶向配体,同一技术平台可针对不同疾病的相关蛋白,大大提高药物研发效率,降低开发成本。
联合治疗策略的创新空间。SPYTACs可与现有疗法形成互补。例如,与BACE抑制剂或γ-分泌酶调节剂联合使用,可能从产生和清除两个环节协同控制Aβ水平。与抗tau疗法结合,可同时针对阿尔茨海默病的两大病理特征。与抗炎药物或神经营养因子联合,可能产生多模式治疗效果。
产业竞争格局的重新塑造。传统制药巨头和新兴生物技术公司都在积极布局SPYTACs领域。罗氏、礼来、渤健等公司在阿尔茨海默病治疗领域有深厚积累,正在评估SPYTACs技术的应用潜力。同时,专注蛋白质降解技术的新锐公司,如Arvinas、C4 Therapeutics等,也在开发神经退行性疾病相关的SPYTACs项目。
结语
SPYTACs技术代表了阿尔茨海默病治疗研究的重要创新方向。通过巧妙结合小分子的血脑屏障穿透能力和蛋白质降解机制,这一技术有望解决传统抗体疗法的关键局限,为清除Aβ提供全新策略。尽管仍需临床试验验证其安全性和疗效,但临床前研究的积极数据已经引起了学术界和产业界的高度关注。
从科学原理到临床应用,从单靶点干预到多靶点协同,SPYTACs技术正在重新定义神经退行性疾病的治疗可能。随着研究的深入和技术的成熟,这种新型治疗模式可能不仅改变阿尔茨海默病的治疗现状,也为整个神经科学领域带来新的启示。未来几年,随着首批临床试验数据的公布,我们将能更清晰地评估这一技术是否真的能开启阿尔茨海默病治疗的“后抗体时代”,为全球数千万患者带来新的希望。
文章来源:征战AD


