2026创新药抗体&ADC合作大会关注到,近期发表于《自然·医学》的研究揭示,在小鼠胰腺癌前病变模型中使用KRAS G12D抑制剂MRTX1133进行早期干预,可使总生存期显著延长超过300%,为胰腺癌的极早期防治提供了新的科学依据。该研究首次在动物模型中证实,在胰腺上皮内瘤变(PanIN)这一公认的癌前病变阶段进行精准靶向治疗,能够有效阻断其向侵袭性胰腺导管腺癌(PDAC)的恶性转化。
一、 研究设计与核心发现
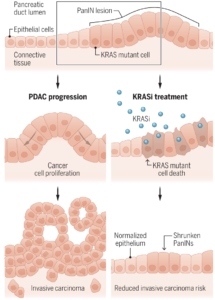
基因工程小鼠模型精准模拟人类病程。研究团队构建了条件性Kras G12D突变小鼠模型,其胰腺病变发展过程与人类高度相似:从正常导管上皮逐步发展为低级别PanIN、高级别PanIN,最终进展为侵袭性PDAC。通过分子影像学和病理学分析,研究者在病变早期(PanIN阶段)即开始给予MRTX1133治疗,避开了传统治疗中肿瘤已形成完整免疫抑制微环境、结构复杂的难题。
生存期数据显示突破性改善。对照组小鼠(未治疗)的中位生存期约为8个月,这与携带KRAS G12D突变小鼠的自然病程一致。而接受MRTX1133早期干预的治疗组,中位生存期延长至24个月以上,超过80%的小鼠在实验观察期内(24个月)未发展成侵袭性癌。部分小鼠甚至在停药后,其PanIN病变保持稳定或出现消退,提示早期干预可能带来持久的生物学改变。
分子与病理机制得到深入阐明。治疗组小鼠的胰腺组织中,与细胞增殖(Ki67)、炎症及纤维化相关的标志物表达显著下调。单细胞RNA测序分析进一步显示,早期使用KRAS抑制剂重塑了肿瘤微环境,减少了免疫抑制性细胞(如髓源性抑制细胞、M2型巨噬细胞)的浸润,同时延缓了致密纤维结缔组织增生(desmoplasia)的形成——这是胰腺癌化疗耐药和免疫逃逸的关键屏障。
二、 科学意义与临床启示
验证“癌前病变干预”新范式。该研究为“在癌症发生之前进行拦截”的预防性治疗策略提供了强有力的临床前概念验证。胰腺癌因早期诊断困难、进展迅速、治疗手段有限而被称为“癌王”,五年生存率不足10%。若能在高危人群(如特定基因突变携带者、慢性胰腺炎患者)中,通过影像或生物标志物筛查出癌前病变并进行药物干预,将有望从根本上改变该病的治疗格局。
明确KRAS靶向治疗的最佳时机。研究提示,KRAS靶向药的疗效高度依赖于疾病阶段。在肿瘤未形成完整、复杂的基质屏障和免疫抑制环境前,KRAS抑制剂能更有效地靶向驱动基因并激发机体抗肿瘤免疫。这解释了为何同类药物在晚期PDAC患者中的疗效相对有限,并为设计联合治疗方案(如KRAS抑制剂联合免疫治疗)提供了新的时间窗口依据。
推动精准早期筛查与预防。研究成果将加速针对KRAS突变高危人群的早期监测方案开发。结合液体活检(检测循环肿瘤DNA或外泌体中的KRAS突变)和先进影像学,有望实现对PanIN的早期发现与分层管理。这为未来开展针对癌前病变的临床试验奠定了理论基础。
图片来源:BioArt
三、 挑战与未来方向
转化至人体的不确定性。小鼠模型与人类在胰腺解剖、免疫系统和疾病进展速度上存在差异。PanIN病变在人体中可能更分散、更不易被早期检测。需要开发更灵敏的无创诊断工具来识别适合干预的高危人群。
长期安全性与耐药性。需评估长期抑制KRAS信号在正常组织中的潜在毒性。尽管早期干预效果显著,但如同所有靶向治疗,耐药性问题可能出现。研究者正在探索间歇给药、联合其他信号通路抑制剂等策略以延缓耐药。
临床路径的构建。如何定义“高危人群”,如何制定干预的启动标准、治疗时长和疗效评估终点,都需要通过严谨的临床试验来探索。这可能催生一类全新的临床研究——癌前病变干预试验。
结语
这项研究标志着胰腺癌防治策略的一个重大思维转变:从治疗晚期疾病转向拦截早期恶变。KRAS抑制剂在癌前病变模型中展现出的惊人疗效,不仅为胰腺癌,也为其他由明确驱动基因突变引发的恶性肿瘤(如肺癌、结直肠癌)的早期防治提供了全新的研发思路。尽管通往临床转化之路仍充满挑战,但这项工作无疑为最终征服“癌王”点燃了一盏新的希望之灯。
文章来源:BioArt


